淺談台灣肺癌篩檢
Lung cancer LDCT screening in Taiwan
文 / 張基晟
肺癌在台灣為死亡率第一、發生率第二的癌症。依據我國最新癌症登記報告,在2021年初次診斷肺癌共計16880人,當年肺癌造成10040人死亡(1)。自2011年至2015年的統計,在台灣有六成的病人初診斷即為第四期的肺癌(2)。因此肺癌的早期診斷一直是大家關心的重要議題。
回顧肺癌篩檢的臨床試驗,2011年刊登在NEJM的NLST trial證實相較於胸部X光的篩檢,低劑量胸部電腦斷層(LDCT)可以早期偵測肺癌並下降20%的肺癌死亡率(3)。隨著台灣民眾對健康議題的了解增加及低劑量胸部電腦斷層的普及,近年來台灣初診斷第一期肺癌的個案數已從2011年的六百多例,上升至2021年的兩千三百多例。但是第四期肺癌的個案數並沒有因此下降,反而從2011年的五千七百多例上升至2021年的的七千五百多例。如此特殊的流行病學表現,值得我們去思考並探討台灣肺癌的成因,以及能否有更好的篩檢方式。
台灣的肺癌與歐美國家的不同,多數患者不曾抽過菸
目前已知的肺癌風險因子包括了:抽菸、肺癌家族史、空汙、氡氣、輻射線暴露、年紀、職業或重金屬暴露等(如:石綿、砷、鎘、鎳等)。歐美國家的肺癌以男性為主、最常見的腫瘤突變為KRAS且有八成以上的個案與抽菸有關。也因此目前世界各國的公衛政策皆著重於抽菸20至30包年(20-30 pack-year)的個案進行早期肺癌篩檢。
然而在台灣,女性和男性罹患肺癌的人數相當,且女性的罹患率呈逐年上升的趨勢。自1995年開始實施菸害防制法及後來推行菸品健康福利捐徵收,台灣的吸菸人口大幅減少(4)。隨著吸菸人口的逐年減少,我國肺腫瘤細胞型態的比例分布也發生了變化。根據癌登資料,與吸菸更為相關的小細胞肺癌及鱗狀上皮肺癌比例自2003年後逐年下降,但肺腺癌的個案數及罹患率卻逐年上升,並自2009年後成為台灣肺癌的主要類型。肺腺癌在台灣最常見的腫瘤突變為表皮生長因子(EGFR)突變,尤其在有肺癌家族史和女性患者中更為顯著,且其中有超過一半的個案(約53%)終其一生都未曾抽過菸。然而,若以其他國家20至30包年抽菸的早期肺癌篩檢標準來看,我國符合條件的新診斷個案僅不到兩成(2)。

台灣的肺癌篩檢
──有肺癌家族史、不抽菸、女性、年紀為肺癌的高危險因子
於2007年至2011年期間經衛福部指導,在台灣多家醫學中心對於有肺癌家族史(生物一等親)的1102位民眾進行前瞻性低劑量電腦斷層的篩檢。相較於美國NLST trial對於抽菸30包年的受試者行低劑量電腦斷層有1.1%的肺癌偵測率(5),研究發現台灣有肺癌家族史的受試者肺癌偵測率為4.5%(50 of 1102)。特別是在具有多重肺癌家族史(家族成員有兩個以上罹患肺癌)、非吸煙者、年輕人以及母親為肺癌患者,罹患肺癌的風險更大。其中同時具有多重肺癌家族史和非吸菸的受試者,其罹癌率竟高達9.4%(6)。
台灣非吸菸者肺癌篩檢試驗(TAiwan Lung cancer scrEening in Never-smoker Trial, TALENT)是於2015至2019年在台灣的17家三級醫學中心進行的全國性、多中心、前瞻性的共同研究。研究總共招募了12011名受試者,其中6,009人有肺癌家族病史。目前共檢測出318例肺癌,罹癌率為2.6%(原位癌佔 0.5%,侵襲性肺癌佔2.1%)。結果顯示在有肺癌家族史的參與者中,侵襲性肺癌的患病率較高。而其中在女性、肺癌家族病史和年紀超過60歲的族群發生肺癌的風險更加相關(7)。
而近期國健署自2022年對重度抽菸(累積超過30包年)及不抽菸但有肺癌家族史這兩種族群進行前瞻性的低劑量電腦斷層肺癌篩檢試驗。收案一年後初步的結果也同樣發現有肺癌家族史的試驗者罹癌率比重度抽菸者來得高(肺癌家族史為1.4%;重度抽菸為0.6%)。

發展台灣的肺癌風險預測模型是必要的
從前述的三項前瞻性臨床試驗可得知,有肺癌家族史的受試者會有較高的肺癌發生率,但並非為台灣肺癌比例佔據最高的誘發因子。根據先前台灣發表的GELAC study,肺癌家族史推測至多僅佔整體肺癌個案數的15%(8)。顯然對於台灣肺癌發生的成因,至今我們仍有許多尚未了解的因素。
為此,台美癌症登月計畫(Cancer Moonshot)進行了一個前瞻性蛋白基因體(proteogenomic)研究。研究發現不抽菸年輕女性的肺癌特徵為高盛行率的APOBEC基因突變;而不抽菸的年長女性肺癌特徵為環境致癌物的過度表現(9)。英國學者Charles Swanton引用了嘉義長庚的資料,推論出空汙會促進肺腺癌的發生,而台灣是研究中PM2.5及肺腺癌發生率最高的國家(10)。
究竟那些族群接受肺癌低劑量電腦斷層篩檢的效益最高?不論是依照美國預防服務工作組(USPSTF)的篩檢標準,或是PLCO風險預測模型皆不能有效地找出我國高肺癌風險的族群。而針先前台灣發表的TNSF-SQ預測模型,加入基因分析後可篩選出易罹患肺癌的不抽菸高風險女性族群(11,12)。但若肺癌篩檢需同時檢測基因及安排電腦斷層,對一個國家公衛篩檢政策而言不是一個便利且符合經濟效益的做法。
目前衛福部補助的癌四計畫FORMOSA trial(Formatting the Risk Models for Never-Smoked Lung Cancer)為前瞻性多中心臨床研究。將統合空汙、重金屬、環境及職業等因素,並使用AI判讀及AI影像預測,進以驗證與優化多面向不抽菸肺癌風險預測模型(MOHW112-TDU-B-222-124019)。期望在不久的將來,能因此研究計畫讓我們對台灣的肺癌成因更加了解,並發展出符合台灣的風險預測模型及適切的肺癌篩檢方式。
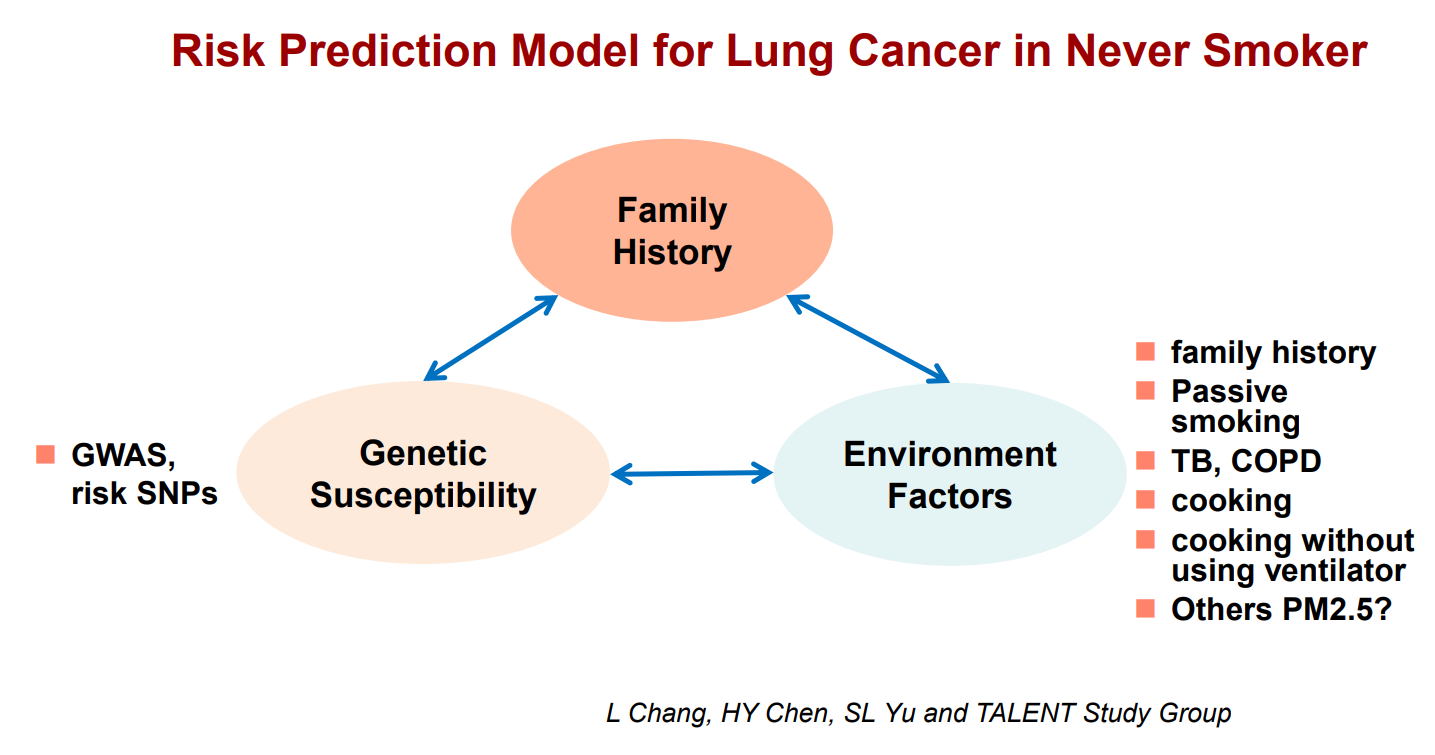
台灣有超過一半的肺癌為非吸菸者,流行病學也與歐美國家迥異。因此發展我國的肺癌風險預測模型,以及為國人量身訂製低劑量電腦斷層篩檢的條件和後續追蹤的方式成了我們迫切需解決的問題。
參考資料:
- 中華民國110年癌症登記報告, CANCER REGISTRY ANNUAL REPORT, 2021 TAIWAN, https://www.hpa.gov.tw/File/Attach/17639/File_23506.pdf
- Tseng CH, Tsuang BJ, Chang GC, et al. The Relationship Between Air Pollution and Lung Cancer in Nonsmokers in Taiwan. J Thorac Oncol. 2019 May;14(5):784-792.
- National Lung Screening Trial Research Team; Aberle DR, Adams AM, Berg CD, et al. Reduced lung-cancer mortality with low-dose computed tomographic screening. N Engl J Med. 2011 Aug 4;365(5):395-409.
- 菸害防治衛生福利部國民健康署https://www.hpa.gov.tw/Pages/List.aspx?nodeid=41
- National Lung Screening Trial Research Team; Church TR, Black WC, Aberle DR, et al. Results of initial low-dose computed tomographic screening for lung cancer. N Engl J Med. 2013 May 23;368(21):1980-91.
- Wang CL, Hsu KH, Chang GC et al. Low-Dose Computed Tomography Screening in Relatives With a Family History of Lung Cancer. J Thorac Oncol. 2023 Nov;18(11):1492-1503.
- Chang GC, Chiu CH, Yang PC et al.; TALENT Investigators. Low-dose CT screening among never-smokers with or without a family history of lung cancer in Taiwan: a prospective cohort study. Lancet Respir Med. 2023 Nov 29:S2213-2600(23)00338-7.
- Lo YL, Hsiao CF, Chang GC, et al. Risk factors for primary lung cancer among never smokers by gender in a matched case-control study. Cancer Causes Control. 2013 Mar;24(3):567-76.
- Chen YJ, Roumeliotis TI, Chang GC, et al. Proteogenomics of Non-smoking Lung Cancer in East Asia Delineates Molecular Signatures of Pathogenesis and Progression. Cell. 2020 Jul 9;182(1):226-244.e17.
- Hill W, Lim EL, Swanton C et al. Lung adenocarcinoma promotion by air pollutants. Nature. 2023 Apr;616(7955):159-167.
- Tammemägi MC, Church TR, Hocking WG, et al. Evaluation of the lung cancer risks at which to screen ever- and never-smokers: screening rules applied to the PLCO and NLST cohorts. PLoS Med. 2014 Dec 2;11(12):e1001764.
- Chien LH, Chen CH, Chang GC et al. Predicting Lung Cancer Occurrence in Never-Smoking Females in Asia: TNSF-SQ, a Prediction Model. Cancer Epidemiol Biomarkers Prev. 2020 Feb;29(2):452-459.